受講生の半分の人には EGFP cDNA を組み込んだ pBluescript II SK+ プラスミド DNA を
渡します。残りの半分の人には,約 700 bp の cDNA を組み込んだ pQE30 プラスミドを
渡します。
1. 1.5 mL エッペンチューブを用意し,以下の試薬を混合して EGFP cDNA 切り出し
用の反応液を作る。
H2O
36 μL
EGFP-pBluescript II SK+ (0.5 μg/μL)
2 μL
10x 制限酵素バッファー (a)
5 μL 10x ウシ血清アルブミン (b)
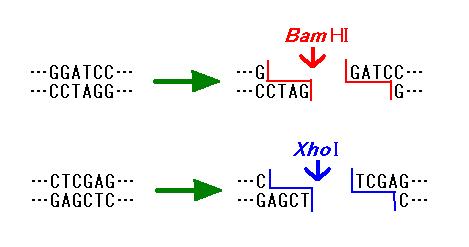
5 μL BamHI (c)
1 μL HindIII (d)
1 μL
2. 1.5 mL エッペンチューブを用意し,以下の試薬を混合して pQE30 切断用の
反応 液を作る。
注: みんなに配る pQE30 には,BamHI 配列と HindIII 配列の間に約 700 bp の
H2O
36 μL
pQE30 (0.5 μg/μL)
2 μL 10x 制限酵素バッファー (a)
5 μL 10x ウシ血清アルブミン (b)
5 μL BamHI (c)
1 μL HindIII (d)
1 μL
cDNA を組み込んであります。みんながほしいのは cDNA ではなくプラスミド
ベクターの方です。切断後は,cDNA の方は捨ててしまいます。
3. 反応液をよく混ぜて,37℃ で約 1 時間、反応させる。
注: 制限酵素はタンパク質なので,凍結融解を繰り返すと立体構造が壊 れて活性
が落ちます。そこで,-30℃ の冷凍庫で凍らないように(また,タンパクが安定に
保たれるように) 50% のグリセリンを含むバッファーに溶か してあります。その
ため,反応液に酵素を入れると酵素はすぐに反応液に混ざらずに底に沈みます。
反応液を作ったときによく混ぜないと反応が進まないので注意。
4. 反応液に,等量の フェノール /クロロホルム混合液 (e) を加えてボルテックス。
注: みんなが使うフェノール/クロロホルム混合液は,水で飽 和させたものであり,
チューブの中で分離していますが,下の黄色い層がフェノール/クロロホルム
なのでそちらを使わなければいけません。
5. 5 分間遠心する。
6. 黄色の下層(有機溶媒の層)と無色の上層(水層)に分離するので,上層を
とっ て新しいエッペンに移す。
注: 遠心後,タンパク質は変性してフェノール/クロロホルム 層と水層の間に白い
沈殿となります。(タンパク量が少ない場合には沈殿が見えない場合もあり
ます。)一方,核酸は水層に残るので,ほしいのは水層です。
間違えないように。
7. 5 μL の 3 M NaOAc (f) と 125 μL のエタノールを加え,よく混ぜる。
注: これがごく標準的なエタノール沈殿(略してエタ沈)。
8. -80℃ に 5 分ほど置いた後,10 分間遠心し,上清を完全に捨てる。
9. 75% エタノールを 200 μL ほど静かに注ぎ込み,再び 1 分ほど遠心。
10. エタノールを完全に捨てる。
11. 沈殿が乾燥したら 10 μL の TE バッファー (g) を加える。
ここまでできたら次のステップへ。。。
10x というのは,反応液中の最終濃度に対して 10 倍の濃度・・・すなわち,10 倍濃縮(b) 10x ウシ血清アルブミン
という意味。メーカーによって組成に多少の違いがあるが,例えばタカラが BamHI 用
に奨める 10x バッファーの組成は [200 mM Tris-HCl (pH 8.5),100 mM MgCl2,10 mM
dithithreitol (DTT),1000 mM KCl]。HindIII 用は [100 mM Tris-HCl (pH 7.5),100 mM
MgCl2,10 mM DTT,500 mM NaCl]。両者の組成は異なるが,HindIII は BamHI 用の
バッファーでもよく切れる。一方,BamHI は HindIII 用のバッファーでは,20% 以下の
相対活性(専用 バッファーで反応したときと比べて,20% 以下の効率でしか標的配列を
切断しない)しか望めない。したがって,今回の実習では BamHI 用のバッファーを
使って,両方の酵素で同時に切断する。
1 mg/mL のウシ血清アルブミンを使う。反応液中の制限酵素は低濃度になるが,ウシ(c) BamHI
血清アルブミンを混ぜておくと酵素タンパクの安定性が増す。酵素によっては添加不要
なのだが,ウシ血清アルブミンを添加することによって活性が阻害されるような制限酵素
はないので(必要か不要かをいちいち考えるのが面倒なので),大抵はウシ血清アルブミン
を含む反応液を作る。
Bacillus amyloliquefaciens H という細菌起源。認識配列は [5'-G/GATCC-3']。(d) HindIII
Bam というのは属名の頭 1 文字と種名の頭 2 文字をとったもの。このように,制限酵素
の名前の頭 3 文字は学名(ラ テン語)に由来するのでイタリックで書く。 4 文字め以降は
イタリックにしない。ちなみに,DNA 上の認識配列を表記するときには BamHI はイタリック
にしない。 BamHI は高濃度のグリセリン,Mn2+ の存在,低イオン強度下で Star 活性が
出ることが知られている。
Haemophilus influenzae Rd という細菌由来。認識配列は [5'-A/AGCTT-3']。(e) フェ ノール/クロロホルム混合液
Mn2+ や DMSO の存在下で Star 活性が 出ることがある。
(f) 3 M NaOAc
3 M の酢酸ナトリウムをこう書く。酢酸ナトリウムの粉を最終濃度 3 M になるように溶かし,(g) TE バッファー
酢酸で pH を 5.2 に合わせたもの。核酸のエタノール沈殿用の塩としては最も一般的に
使われる。エタノール沈殿のときは 0.3 M になるように核酸溶液に加え,さらに 2〜2.5
倍量のエタノールを加えて核酸を沈殿させる。(RNA の場合は 3 倍量のエタノールを
使用する)
(h) フェノール