まず、皆さんの試料 D (一番左は試料 A )

次に,電気泳動の後の作業について紹介します。
1. コテを使って,2枚のガラス板の間に隙間を作る。
2. ガラス板の一方を外す。ゲルを破らないように丁寧に。
3. ゲルを破らないようにタッパーに移す。
4. ゲルを染色液にひたす。染色。
5. 余分な染色を脱色する。
1 2


3 4


5

染色に使った溶液は以下の通りです。
* 染色液: クマシーブリリアントブルー(Coomassie Brilliant Blue: CBBと略す)
45% メタノール(v/v),10% 酢酸(v/v) に対して,CBB の粉を
0.25% (w/v)になるように溶かしたものです。
* 脱色液: 25% メタノール(v/v),10% 酢酸(v/v),2.5% グリセリン(v/v) です。
【染色の詳しい手順】
(1) 泳動後のゲルをゲル板から外し,CBB 染色液に浸ける。
(2) 染色時間を短縮するために電子レンジ 1 分くらい加熱。
(急がないなら,シェイカーでゆっくり揺すりながら,室温に 1〜 時間置く。)
(3) 染色液をビンに戻し,ゲルを水道水で洗う (水が青くならなくなるまで)。
(4) 脱色液に浸け,ゆっくり揺すりながら,室温で数時間から一晩置く (バンドが
はっきりと見えてくるまで)。
(5) 10% 酢酸水溶液に浸け,室温で静置する (ゲルのバックグラウンド=背景の
青い色がすっかり抜けるまで)。
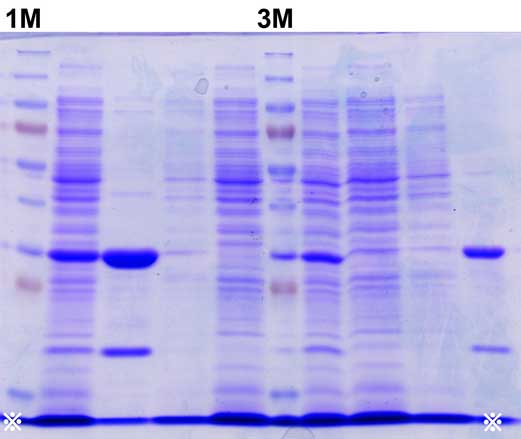
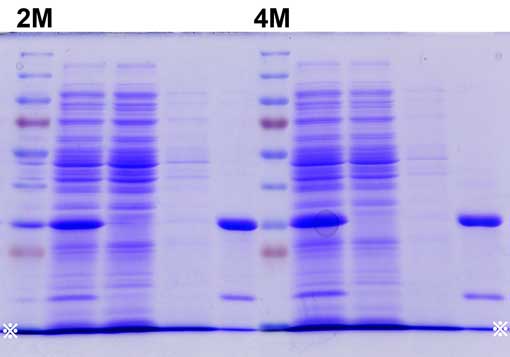
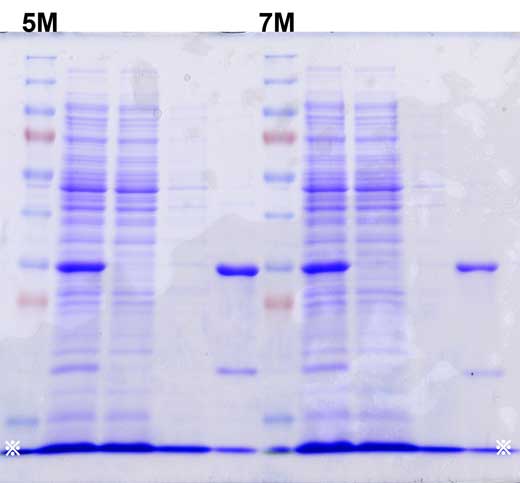
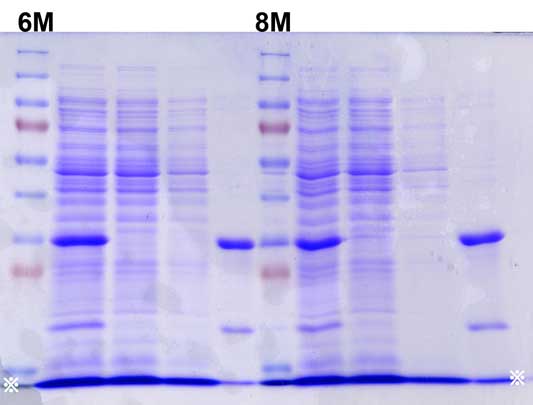
ここからが電気泳動の結果です。
M レーンでは,マーカーを電気泳動しました。各バンドの分子量がいくらかは,
以下の web サイトを参考にしてください。
マーカーの情報は,こちらから。メーカーの HP にとびます。
「Triple-color」の方です。2 本あるオレンジのバンドを目印にしてください。
一番低分子量の 10 kDa を示す緑色のバンドは見えません。※のあたりに
ありますが,今回は見えなくなっています。
※注意!
全てのゲルの写真の中で低分子量の位置に太いバンドがあります。
写真の左右の下端のあたりに「※印」をつけてあります。その「※印」を
つないだ線上にあるバンドです。隣あうレーン同士でつながってしまって
いるので,バンドには見えないですね。全部のレーンで見えてます。
このバンドは,mCherry タンパク質ではありません!
このバンドの正体は,大腸菌からタンパク質を取り出す時に使った
リゾチームという酵素(タンパク質)です。リゾチームで大腸菌の細胞壁を
壊し,大腸菌からタンパク質を取り出しやすくしました。
アフィニティクロマトグラフィーの仕組みを考えれば,リゾチームは mCherry
の精製を邪魔しません。なので,使っても問題ないです。 溶出液 「d」 の
レーンで見えてしまっているのは,使ったリゾチーム量が多すぎて,洗いきれ
なかったことが原因です。なので,「※」位置にバンドがあることについては,
頭を悩ませる必要はありません。それ以外のバンドをよく見ましょう。
もしも,この web ページや授業で手に入れた情報以外で,「考察」のために欲しい
情報があれば,是非問いあわせて下さい(課題の答えは教えてあげませんが,
ヒントになりそうなことは教えてあげます)。
わからないことがあれば,砂長か藤原先生か TA まで,いつでも質問に来てください。